La medicina del futur
En una escena de la sèrie de dibuixos animats “Els Supersònics”, es podia veure al metge de capçalera de la família fent una consulta en línia al fill. És una sèrie dels anys seixanta, i estaven fent una encertada predicció d’un futur que ja estem vivint.
A la pel·lícula “Viaje alucinante”, també dels anys seixanta, un submarí d’exploracions oceàniques és miniaturitzat, juntament amb els seus cinc tripulants, i introduït dins del cos d’un científic per salvar-li la vida. En aquest cas la predicció no s’ha complert. O no del tot.
Quins són els avenços que podem preveure en el món de la medicina a curt termini? La miniaturització o, millor dit, la nanotecnologia, és un d’ells.
Nanotecnologia
Quan es parla de nanotecnologia es parla de coses extremadament petites. Per fer-nos una idea de les dimensions, en un nanòmetre hi caben entre tres i cinc àtoms.
La nanotecnologia encara no permetre reduir ni al Stephen Boyd ni a la Raquel Welch, protagonistes de la pel·lícula del submarí. Però sí que permet construir robots, anomenats nanobots, de la mida del submarí (que són mil vegades més petits que el gruix d’un cabell), tot i que molt més rudimentaris.
Un exemple ben conegut d’utilització de la nanotecnologia és el de les vacunes d’ARN missatger de Pfizer-Biontech i Moderna. En aquestes vacunes l’ARN missatger s’introdueix en nanopartícules que són les que els transportaran. En aquest cas només són petites gotetes de greix, res semblant a un robot autònom. Aquestes gotetes tenen l’enorme avantatge que, en ser dissenyades químicament, són acceptades pel cos. No passa el mateix amb les vacunes que fan servir un vector viral (un altre virus) com en les d’Oxford i Astra Zeneca per transportar el material viral de la Covid.
S’està treballant en una fase de laboratori amb nanobots més complexos que la nanogoteta. Entre altres coses, s’està experimentant amb nanobots que podrien portar medicaments fins a cèl·lules canceroses per destruir-les. A la Universitat Northwestern fan servir unes nanopartícules d’or, en forma d’estrella, que se senten atretes per una proteïna a la superfície de la cèl·lula cancerosa que les trasllada al nucli de la cèl·lula. I allà alliberen el fàrmac per fer la seva funció.
Entre els problemes que s’estan trobant els investigadors està desenvolupar un sistema eficient de moviment autònom dels nanobots, trobar un sistema de navegació d’aquests dins del cos, i eliminar els possibles components dels robots un cop han acabat la seva feina. En el cas de les vacunes no s’han trobat cap d’aquests problemes perquè n’hi havia prou en arribar a algunes cèl·lules del braç i perquè la coberta és una simple goteta de greix que s’elimina fàcilment.
Una segona línia d’investigació és el de crear nanofàbriques, les quals produirien compostos de proteïnes o medicaments sota demanda, justament en el lloc on hi ha la malaltia.
Una tercera línia d’investigació està relacionada amb les nanofibres, amb fibres de diàmetres inferiors als mil nanòmetres, amb utilitats per apòsits, teixits quirúrgics, materials per a implants, enginyeria de teixits i components d’òrgans artificials.
CRISPR
Resumidament, podríem dir que és una tècnica que permet fer modificacions a l’ADN de forma quirúrgica. I, modificant l’ADN de les cèl·lules, estem canviant el seu funcionament. Seria com portar el cotxe al taller quan té alguna cosa que no funciona bé. Se li obre el capó i se li arregla la peça que calgui.
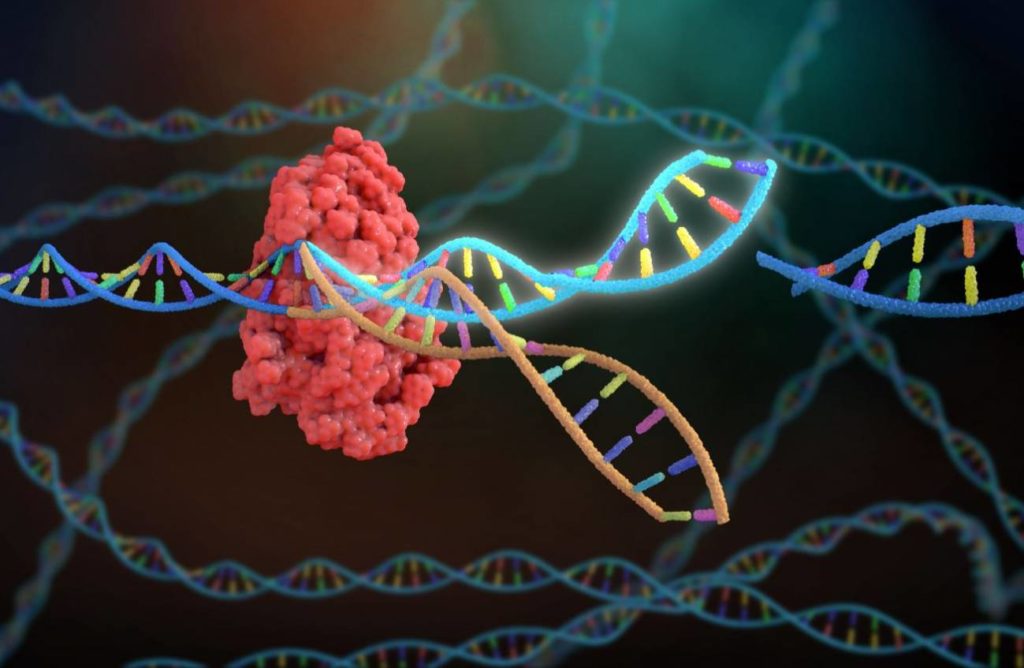
És una de les línies de treball més esperançadores per al tractament de malalties hereditàries, mitjançant la modificació de les mutacions genètiques que les provoquen. I també del tractament del càncer i, segurament, d’altres malalties adquirides.
El primer article sobre el CRISPR es va publicar el 2012. Es va descobrir com a resultat de l’estudi del sistema immune que tenen els bacteris per protegir-se dels virus. Fins aquell moment es creia que els bacteris només tenien un sistema immune innat rudimentari. Però es va veure que tenien un sistema molt més complex, amb unes proteïnes que actuen com a tisores moleculars per tallar les cadenes dels virus. Doncs bé, aquestes tisores es poden utilitzar per fer modificacions concretes en l’ADN. Són la base d’aquesta tècnica. Després es descobririen altres proteïnes no tallants que es podrien fer servir per fer modificacions sense trencar la cadena d’ADN.
No fa tant de temps que es coneix l’ADN humà complet. La seva seqüenciació és del 2001, quan es va publicar l’ordre de les seves lletres (les “lletres” són en realitat els quatre compostos químics que formen l’ADN: Adenina, Timina, Citosina i Guanina, i que van un darrere l’altre). Té molt de mèrit considerant que l’ADN humà té uns 3200 milions de lletres, repartides entre 23 parells de cromosomes.
Avui en dia, un dels principals problemes amb els quals es troben els científics és el de l’administració clínica. A una persona adulta, caldria introduir-li suficient quantitat de CRISPR al cos perquè modifiqués suficients cèl·lules per ser efectiu, i que això no tingués efectes secundaris. I cal tenir en compte que al cos hi ha uns trenta milions de milions de cèl·lules.
A nivell més localitzat ja s’ha demostrat efectiu, com per exemple en el cas de la immunoteràpia per al tractament del càncer. En aquest cas es milloren algunes cèl·lules humanes del sistema immune, i se li afegeixen marcadors que facin que trobin cèl·lules canceroses i les ataquin.
A banda del sector mèdic, molt probablement s’acabarà utilitzant en la indústria alimentària per millorar plantes i animals. A diferència dels transgènics, aquestes modificacions no tenen cap part d’ADN aliè ni senyals d’intervenció. De fet, les modificacions que es puguin fer amb aquesta tecnologia donen els mateixos resultats que les mutacions aleatòries que fan evolucionar les espècies, tot i que més ràpid i controlat.
CRISPR prové de l’acrònim en anglès. Traduït significa “repeticions palindròmiques curtes agrupades i regularment interespaiades”.
Intel·ligència artificial
L’any passat, investigadors de l’Hospital Clínic i de l’Institut d’Investigacions Biomèdiques August Pi i Sunyer van aconseguir reduir en més d’un 50% la mortalitat dels pacients de Covid a l’hospital, gràcies a una eina d’intel·ligència artificial. Aquesta eina és com un Doctor House (o un Good Doctor) que indica el que s’ha de fer amb cada pacient i en cada moment. A diferència dels metges de les sèries, a aquesta eina se l’alimenta amb milions de dades, de milers de pacients, i les pot tenir totes en compte a l’hora de decidir. I decideix molt de pressa. Això si, li falta la intuïció que demostren aquests personatges de les sèries.

Per tal que aquests models basats en xarxes neuronals siguin efectius cal que siguin entrenats amb grans quantitats de dades. Així, el que fan és aprendre a distingir entre el que és important i el que és superflu, i establir correlacions entre esdeveniments que se li poden haver passat per alt als metges. Requereixen, lògicament, una gran capacitat de càlcul. En el cas del Clínic es va fer servir el superordinador MareNostrum 4 del Barcelona Computing Center.
Una de les principals dificultats d’aquestes eines és l’alimentació de les dades. És fonamental utilitzar com més dades millor, independentment de si, des d’un punt de vista mèdic, es creu que hi tenen relació o no. Això és el que ha de determinar l’eina. Cal afegir dades dels informes de laboratori, de radiologia, de diagnòstics, de cursos clínics, etc. Per això es fan servir tècniques de processament de llenguatge natural (una altra branca de la Intel·ligència Artificial) que analitzen els texts redactats pel personal sanitari i els converteixen en esdeveniments (símptomes, tractaments, evolució, etc.). Donats els resultats obtinguts en el cas de la Covid, ben segur que la Intel·ligència Artificial es farà servir per a moltes altres malalties.
La intel·ligència artificial es pot fer servir per a moltes altres funcions. Per posar un cas ben diferent, a Dinamarca fan servir una tecnologia d’assistència de veu (anomenada Corti) que escolta les trucades d’emergència i subministren informació addicional al personal que està al telèfon per facilitar la presa de decisions.
Robòtica
Actualment, la robòtica està molt implantada en el camp de cirurgia. Permet augmentar la precisió i aplicar un tractament menys invasiu. Les grans cicatrius externes han quedat en el passat per a moltes de les intervencions actuals.
Les pròtesis intel·ligents permetran cobrir els moviments deficitaris. Ja existeixen mans biòniques amb catorze posicions i formes d’agafar les coses. Aquestes són ja capaces de trencar ous, fer servir un ratolí d’ordinador o sostenir ampolles de vidre sense trencar-les. S’està experimentant ja amb mans que transmeten sensacions, connectant sensors als nervis del braç. També s’estan desenvolupant diferents tipus d’exoesquelets per permetre els moviments a persones amb problemes de mobilitat. Fins i tot s’està experimentant amb ulls biònics que, connectats amb el cervell, han permès recuperar la visió, tot i que de forma molt rudimentària. I pel futur s’està treballant ja a desenvolupar òrgans biònics.
Els robots assistencials per a persones malaltes, discapacitades o d’edat avançada encara estan poc desenvolupats. S’espera que puguin fer tasques de neteja, administració de medicaments, supervisió de constants, alimentació, mobilització, etc.
Impressió 3D
Ja s’està utilitzant aquesta tecnologia per fer models anatòmics impresos en 3D per preparar les operacions, sobretot per les que tenen una certa complexitat i impliquen diferents persones a l’equip de quiròfan. També s’han començat a usar per disposar de dispositius mèdics i instruments quirúrgics més precisos, i de més baix cost. Precisament, el seu baix cost fa que també es puguin oferir pròtesis, ortesis i plantilles veritablement assequibles.

Ja s’han imprès teixits vius, per evitar haver de recórrer a autoempelts o a trasplantaments. Per a això es fa servir la bioimpressió, la qual permet incorporar materials biològics, bioquímics i cèl·lules vives. La “tinta” del cartutx de la impressora és en realitat una “biotinta”, un líquid amb cèl·lules, matrius i nutrients. Un cop s’ha bioimprès, es té un teixit en estat d’esbós, el qual es transfereix a una incubadora, per fer que les cèl·lules que contenen madurin per fer el teixit definitiu.
La principal dificultat amb la qual s’estan trobant és la connexió de les estructures impreses als sistemes vasculars, els encarregats de portar la sang a to el cos. Per poder obtenir un òrgan complet, com per exemple un cor, cal que compleixi els requeriments estructurals, però també que tingui la vascularització, la càrrega mecànica i la propagació de senyals elèctrics.
Un futur sempre està en construcció.